Entenda o que é a tabela periódica dos elementos químicos, como ela está organizada e o que são os períodos e as famílias.
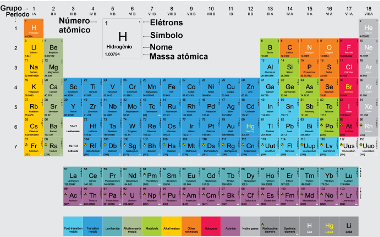
A Tabela Periódica é uma forma de organizar todos os elementos químicos de acordo com as suas propriedades e de mostrar algumas informações sobre eles.
No cotidiano, a organização é muito importante para facilitar a nossa vida. Por exemplo, imagine o seu guarda-roupa bagunçado, com meias misturadas com camisas e calças. Ficaria muito difícil e demoraria mais para encontrar alguma meia específica que você quisesse usar, não é mesmo?! Mas se você organizar o seu guarda-roupa e colocar todas as meias em uma só gaveta, ter uma gaveta para camisetas, outra para bermudas e assim por diante, ficará muito mais fácil encontrar o que precisa. E quanto mais roupas você possui, mais a organização é necessária.
Do mesmo modo, os cientistas foram descobrindo muitos elementos químicos com o passar do tempo. Para você ter uma ideia, em 1850, eram conhecidos cerca de 60 elementos, mas hoje sabemos da existência de 118. Assim, surgiu a necessidade de organizar esses elementos químicos de uma forma que tornasse mais fácil a compreensão de suas propriedades. Esse é o papel da Tabela Periódica dos elementos químicos.
A Tabela Periódica que usamos hoje é organizada em linhas horizontais em ordem crescente de número atômico.
Você deve consultar a Tabela Periódica como se estivesse lendo um texto normal, ou seja, você sempre começa pela primeira linha e do lado esquerdo para o direito e depois segue descendo para as próximas linhas. Os elementos químicos foram colocados na Tabela Periódica em quadradinhos separados, onde o símbolo do elemento fica no meio e o valor do número atômico fica escrito geralmente na parte de cima, como mostra o exemplo do hidrogênio a seguir:

Símbolo do hidrogênio e seu número atômico conforme aparece na Tabela Periódica
O número atômico é a quantidade de prótons ou cargas positivas que os átomos do elemento têm. Esse valor é igual ao número de elétrons quando o átomo está em seu estado fundamental. O hidrogênio é um elemento que só tem 1 próton, ou seja, seu número atômico é 1. Por isso, o hidrogênio é o primeiro elemento colocado na Tabela. O próximo elemento que está na mesma linha que o hidrogênio é o hélio, porque ele possui número atômico igual a 2.
Passando para a linha de baixo, o primeiro é o Lítio com número atômico igual a 3, ao lado dele tem o Berílio com número atômico 4 e assim por diante. Veja as primeiras linhas da Tabela Periódica mostradas abaixo e veja que a ordem do número atômico vai crescendo certinho.

Duas primeiras linhas da Tabela Periódica
Existem sete linhas na Tabela Periódica e essas linhas são chamadas de períodos. Veja:
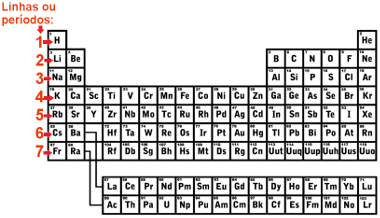
Períodos da Tabela Periódica
Existem 18 colunas que são chamadas de famílias ou grupos. Um aspecto importante é que os elementos que pertecem à mesma família são aqueles que possuem propriedades físicas e químicas semelhantes.
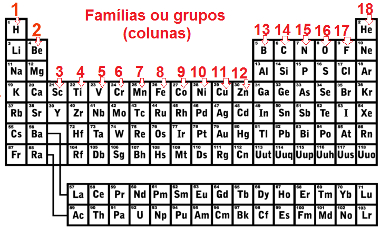
Famílias ou grupos da Tabela Periódica
Vamos ver se você entendeu? Me diga qual é o elemento químico pertencente ao 4º período e à família 16?
Se você disse Se (selênio), acertou! Agora me diga qual é o número atômico dele. Isso mesmo, é 34.
Em cada quadradinho que vem o elemento também se encontram outras informações importantes, como a massa atômica e os elétrons que estão em cada camada eletrônica dos átomos. Por exemplo, veja na imagem a seguir que o neônio tem como símbolo o Ne, seu número atômico é igual a 10, sua massa atômica é igual a 20,1797 u e seus elétrons estão distribuídos assim nas suas camadas: 2 – 8, ou seja, na camada mais próxima do núcleo há dois elétrons e na mais afastada há oito elétrons.

Símbolo do neônio na Tabela Periódica e seu átomo
Agora observe dois aspectos interessantes: (1) o neônio só possui duas órbitas ou camadas onde ficam seus elétrons, é por isso que ele ocupa o 2º período (2ª linha); e (2) ele possui oito elétrons na última camada, é por isso que ele é da família 18.
Isso nos mostra o seguinte:
* Os elementos que estão em um mesmo período da tabela periódica possuem a mesma quantidade de camadas eletrônicas, sendo que podem ter no máximo sete;
* Os elementos químicos que estão em uma mesma família da tabela periódica possuem a mesma quantidade de elétrons na última camada eletrônica:
*Família 1: Possuem todos 1 elétron na última camada eletrônica;
*Família 2: Possuem todos 2 elétrons na última camada eletrônica;
*Família 13: Possuem todos 3 elétrons na última camada eletrônica;
*Família 14: Possuem todos 4 elétrons na última camada eletrônica;
*Família 15: Possuem todos 5 elétrons na última camada eletrônica;
*Família 16: Possuem todos 6 elétrons na última camada eletrônica;
*Família 17: Possuem todos 7 elétrons na última camada eletrônica;
*Família 18: Possuem todos 8 elétrons na última camada eletrônica.
Alguns grupos ou famílias da Tabela Periódica recebem nomes específicos, veja alguns:
Família 1: Metais alcalinos;
Família 2: Metais alcalinoterrosos;
Família 16: Calcogênios;
Família 17: Halogênios;
Família 18: Gases Nobres.

Organização das famílias da tabela periódica
Novamente vamos testar seus conhecimentos. Responda às perguntas a seguir apenas consultando a Tabela Periódica:
1- Qual é o nome da família do cloro?
2- Qual é o seu número atômico e sua massa atômica?
3- Quantas camadas eletrônicas um átomo de cloro possui?
4- Quantos elétrons um átomo de cloro possui na sua última camada eletrônica?
Respostas:
1- Halogênios (família 17).
2- O número atômico do cloro é 17 e sua massa atômica é igual a 35,45 u.
3- Um átomo de cloro possui três camadas eletrônicas porque ele pertence ao 3º período da Tabela.
4- Um átomo de cloro possui sete elétrons na camada de valência porque ele pertence à família 17.
Existem ainda outras informações importantes que a Tabela Periódica nos transmite e que falaremos melhor em textos posteriores. Mas as que tratamos aqui são as principais para você começar a entender como os elementos estão organizados nela. Lembre-se de que uma tabela não é feita para decorar, mas você deve conhecê-la bem para conseguir consultá-la quando necessário.
Por Jennifer Fogaça
Graduada em Química
Aproveite para conferir nossas videoaulas relacionadas ao assunto: